- Là phương pháp dùng hóa chất, các phản ứng hóa học trong quá trình xử lý nước.
- Nếu nước có độ đục lớn chứng tỏ chứa nhiều chất hữu cơ và sinh vật phù du thì dùng phèn và chất tạo keo tụ để ngưng tạp chất.
- Nước chứa nhiều ion kim loại (độ cứng lớn) xử lý bằng vôi, sôđa hoặc dùng phương pháp trao đổi ion. Nước chứa nhiều độc tố H2S xử lý bằng phương pháp oxy hóa, clo hóa, phèn.
- Nước chứa nhiều vi khuẩn thì phải khử trùng bằng các hợp chất chứa clo, ozon.
- Nước chứa Fe thì oxy hóa Fe2+ bằng oxy không khí (làm thóang giàn mưa) hoặc dùng chất oxy hóa để xử lý…
- Độ kiềm của nước nhỏ làm cho quá trình keo tụ khó khăn, nước có mùi vị thì phải kiềm hóa bằng amoniac (NH3). Sau khi cacbon hóa, clo hóa sơ bộ rồi thêm KMnO4.
- Nước có nhiều oxy hòa tan thì phải xử lý bằng cách dùng các chất khử để liên kết oxy. Đó là hydrazin, natrithisunfat…
- Nhìn chung các phương pháp xử lý hóa học thường đạt năng suất và có hiệu quả cao.

3. Xử lý bằng phương pháp sinh học
- Trên thế giới hiện nay phương pháp xử lý nước bằng vi sinh đang được nghiên cứu và có một số nơi đã áp dụng. Trong phương pháp này một số chủng loại vi sinh đặc biệt đã được nuôi cấy và được đưa vào trong quá trìng xử lý nước với liều lượng rất nhỏ nhưng đạt hiệu quả cao. Tuy nhiên cho đến nay những kết quả nghiên cứu của phương pháp này chưa được công bố rộng rãi.
- Tùy thuộc vào nguồn nước làm nguyên liệu cho các lãnh vực khác nhau mà ngườt ta đã sử dung các phương pháp khác nhau để xử lý nước cấp cho lãnnh vực đó. Thông thường thì người ta kết hợp cả 2 phương pháp cơ học và hóa học để xử lý nước.
II. CÔNG NGHỆ MÀNG SIÊU LỌC
1. Giới thiệu về công nghệ màng siêu lọc:
Màng lọc UF hay còn gọi là màng siêu lọc sợi rỗng thẩm thấu, quá trình lọc sẽ cho phép nước đi từ ngoài vào bên trong sợi rỗng nhờ áp lực dòng chảy của nước. Đây được xem là công nghệ lọc nước quan trọng được sử dụng để sản xuất nước tinh khiết cao.

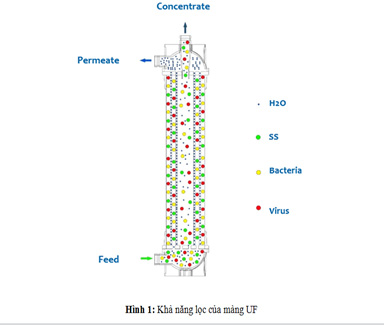
Màng lọc UF có hiệu quả trong việc loại bỏ các chất keo, protein, vi khuẩn và các phân tử hữu cơ có kích thước lớn hơn 0.01 micron.
2. Cấu tạo module màng siêu lọc UF
Màng siêu lọc UF là một tổ hợp các sợi rỗng bằng vật liệu PVDF (PolyVinyliden DiFlorua) với kích thước lỗ lọc cực nhỏ 0.01 micron. Ứng dụng loại màng UF trong thiết kế hệ thống xử lý nước đã mang lại:
- Hiệu suất lọc tuyệt vời với thông lượng cao và ổn định.
- Khả năng loại bỏ được nhiều loại vi khuẩn/virus đã được chứng minh qua nhiều công trình thực tế.
- Chi phí đầu tư hợp lý.
- Kích thước của hệ thống gọn nhỏ, cấu trúc đơn giản nên không tốn mặt bằng lắp đặt.
- Quá trình lọc diễn ra ở nhiệt độ bình thường và áp suất thấp nên tiêu thụ ít điện năng.
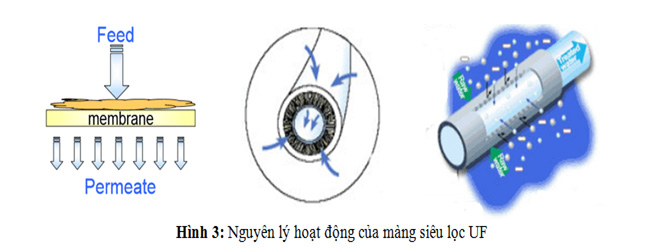
3. Nguyên lý hoạt động của màng siêu lọc UF
Màng lọc UF hoạt động trên cơ chế chuyển động của các phần tử nước, nhờ áp lực bên ngoài tạo ra một dòng chảy mạnh (có thể gọi là quá trình phân ly trong chính dòng nước ở môi trường bình thường nhờ áp lực). Khi đó sẽ đẩy các thành phần hóa học, các kim loại, tạp chất có trong nước sang vùng có áp lực thấp hay trôi theo dòng nước ra ngoài theo đường thải. Các phần tử có kích thước > 0.01 micron sẽ bị giữ lại.
III. XỬ LÝ NƯỚC NHIỄM AMONI, NITRAT
1. Khử Amoni
1.1. Phương pháp Clo hóa nước đến điểm đột biến
Khi cho CLo vào nước, trong nước tạo ra axit hypoclorit
Cl2 + H2O ⇔ HCl + HOCl
Axit hypoclorit kết hợp với NH4+ tạo thành Cloramin. Khi nhiệt độ nước ≥200C, pH ≥7 phản ứng diễn ra như sau:
OH- + NH4+→ NH4OH ⇔ NH3 + H2O
NH3 + HOCl → NH2Cl + H2O monocloramin
NH2Cl + HOCl → NHCl2 + H2O dicloramin
NHCl2 + HOCl → NCl3 + H2O tricloramin
Quá trình kết thúc sau 3 phút khuậy trộn nhẹ. Tại điểm oxy hóa hết Cloramin và trong nước xuất hiện Clo tự do gọi là điểm đột biến.NSau khi khử hết NH4+ trong nước cò lại lượng clo dư lớn, phải khử clo dư trước khi cấp cho người tiêu thụ.
Khử Clo dư trong nước sau khi lọc bằng Natrisunfit (Na2SO3)
Na2SO3 + Cl2 + H2O → 2HCl + Na2SO4
Khử Clo dư trong nước sau khi lọc bằng Trionatrisunfit (Na2S2O3)
4Cl2 + Na2S2O3 + 5H2O → 2NaCl+ 6HCl + 2H2SO4
Quá trình diễn ra hoàn chỉnh sau 15 phút khuấy trộn đều hóa chất và nước
1.2. Phương pháp làm thoáng
Muốn khử NH4+ ra khỏi nước bằng phương pháp làm thoáng, phải đưa pH của nước nguồn lên 10.5 – 11.0 để biến 99% NH4+ thành khí NH3 hòa tan trong nước.
Nâng pH của nước thô: Để nâng pH của nước thô lên 10.5 – 11.0 thường dùng vôi hoặc xút. Sau bể lọc pha axit vào nước để đưa pH từ 10.5 – 11.0 xuống còn 7.5
Tháp làm thoáng khử khí amoniac NH3 thường được thiết kế để khử khí amoniac có hàm lượng đầu vào 20 – 40 mg/l, đầu ra khỏi giàn hàm lượng còn lại 1 – 2mg/l, như vậy hiệu quả khử khí của tháp phải đạt 90 – 95%. Hiệu quả khử khí NH3 của tháp làm thoáng khi pH ≥11 phụ thuộc nhiều nhiệt độ của nước. Khi nhiệt độ nước tăng, tốc độ và số lượng ion NH4 chuyển hóa thành NH3 tăng nhanh.
1.3. Phương pháp trao đổi ion
Để khử NH4+ ra khỏi nước có thể áp dụng phương pháp lọc qua bể lọc cationit. Qua bể lọc cationit, lớp lọc sẽ giữ lại ion NH4+ hòa tan trong nước trên bề mặt hạt và cho vào nước ion Na+. Để khử NH4+ phải giữ pH của nước nguồn lớn hơn 4 và nhỏ hơn 8. Vì khi pH ≤ 4, hạt lọc cationit sẽ giữ lại cả ion H+ làm giảm hiệu quả khử NH4+ . Khi pH > 8 một phần ion NH4+ chuyển thành NH3 dạng khí hòa tan không có tác dụng với hạt cationit.
1.4. Phương pháp sinh học
Lọc nước đã được khử hết sắt và cặn bẩn qua bể lọc chậm hoặc bể lọc nhanh, thổi khí liên tục từ dưới lên. Do quá trình hoạt động vi khuẩn Nitrosomonas oxi hóa NH4+ thành NO2- và vi khuẩn Nitrobacter oxy hóa NO2-thành NO3- . Quá trình diễn ra theo phương trình:
NH4+ + 2O2 → NO3- + 2H+ + H2O
1.02NH4++ 1.89O2 + 2.02HCO3- → 0.21C5H7O2N + 1.0NO3- + 1.92 H2CO3 + 1.06H2O
2. Khử Nitrate NO3
Để khử nitrat dùng lọc thẩm thấu ngược RO, điện phân, trao đổi ion trong các bể lọc ionit.
Điều kiện áp dụng phương pháp trao đổi ion
Nước có hàm lượng cặn < 1mg/l.
Tổng hàm lượng ion NO3- và SO42- và Cl- có sẵn trong nước phải nhỏ hơn 250 mg/l là hàm lượng ion Cl- lớn nhất cho phép có trong nước ăn uống. Vì khi lọc qua bể lọc anionit các ion SO42-, NO3- được giữ lại, thay bằng ion Cl- khi hoàn nguyên bể lọc anionit bằng dung dịch muối ăn.